Covid-19: wat zijn de zwakke punten van het SARS-CoV-2 coronavirus?
We zijn in oorlog, aldus de Nederlandse en Belgische regeringen. De ene draconische maatregel van de regering volgt de andere op, hierbij aangevuurd door de rechts-populistische oppositiepartijen. Een oorlog win je alleen als je je vijand door en door kent. Wat is het SARS-CoV-2 coronavirus, dat Covid-19 veroorzaakt?
Virussen
Virussen zijn pakketjes genetisch materiaal (DNA of RNA) die omgeven worden door een eiwitmantel. Worden ze dat niet, dan spreken we over een viroïde, bijvoorbeeld het aardappelspindelknolviroïde, na het prion (besmettelijk eiwit) met rond de 400 nucleotiden (DNA of RNA ‘letters’) de kleinste ziekteverwekker die we kennen. Ter geruststelling: viroïden komen voor zover bekend alleen bij planten voor.
De groep virussen zal vermoedelijk in de toekomst verdere afsplitsingen krijgen: zo zijn er “virussen” zoals de familie van de mimivirussen die eigenlijk meer zwervende celkernen zijn dan ‘dode’ pakketjes genetisch materiaal.
Covid-19 en SARS-CoV-2
Covid-19 is de officiële benaming voor de ziekte die door SARS-CoV-2 wordt veroorzaakt. SARS-CoV-2, doorgaans ‘het coronavirus’ genoemd, is een RNA-virus behorende tot de zeer grote familie van coronavirussen. Virus is de benaming voor de gehele soort, een afzonderlijk virusdeeltje wordt aangeduid met virion.
We worden geregeld geïnfecteerd met coronavirussen. Ze zijn de voornaamste veroorzakers van verkoudheid. Het influenza (griep)-virus, vaak verward met het coronavirus door onder meer de Usaanse president Donald Trump, behoort tot een totaal andere klasse virussen, de orthomyxoviridae (ook RNA-virussen, maar hiermee houdt de gelijkenis op).
Hoe vermenigvuldigen coronavirussen zich?
Alle hierboven genoemde objecten hebben gemeen, dat ze zichzelf niet kunnen vermenigvuldigen zonder een gastheercel. (Een viroïde kan dat soms wel, door middel van RNA-recombinatie in een geschikte voedingsoplossing). Daarom denken sommige biologen, dat het eerste leven een soort viroïde was.
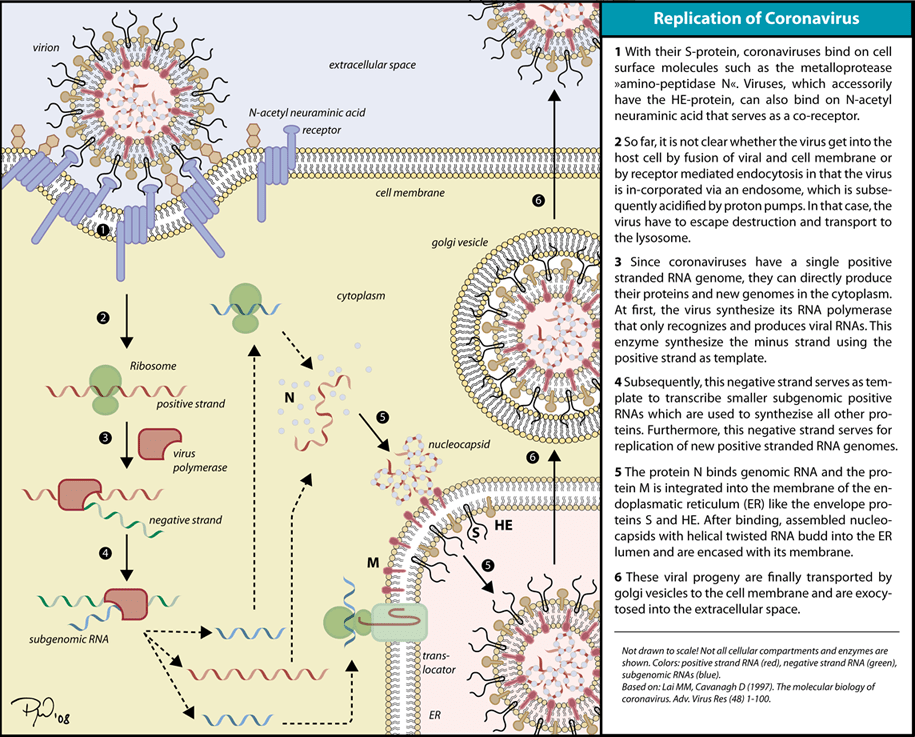
Virions kunnen alleen door hun enorme aantal een gastheercel tegenkomen. Treft een corona-virion een passende receptor, dan bindt het deeltje zich aan deze receptor, zie 1 in de afbeelding. In het geval van het SARS-CoV-2 coronavirus, bindt een ‘stekel’ aan het coronavirion zich aan de geschikte receptor van een menselijke cel (de ACE2-receptor). Vervolgens: hetzij smelt de eiwitmantel van het virion samen met het celmembraan, hetzij komt het binnen via een gespecialiseerde importstructuur, het endosoom. Virologen weten nog niet welke van deze twee mechanismen.
Hierbij komt het virus-RNA in de cel terecht en wordt afgelezen door een ribosoom, dat het RNA van het virion vertaalt in het werkpaard voor het virus: het enzym virus-RNA-polymerase. Dit molecuul, dat alleen reageert op coronavirus-RNA, gaat vervolgens eindeloos veel kopieën maken van dit RNA. Deze vormen het spiegelbeeld van de oorspronkelijke RNA-keten. Deze ‘negatieve’ spiegelbeelden worden door ribosomen vertaald in virus-manteleiwitten en ook weer terugvertaald in ‘positief’ virus-RNA. Vervolgens wordt het virus-RNA ingepakt in de viruseiwitten in het cellulaire transportnetwerk, het ER en via het Golgi apparaat uit de cel getransporteerd.
Hoe kunnen we het Covid-19 virus SARS-CoV-2 saboteren?
Hier zien we meteen wat de zwakke punten zijn van coronavirussen. De mantel van corona-virions bestaat uit eiwitten en lipiden (vetten). Dat maakt ze erg gevoelig voor reiniging met zeep. Zeep vernietigt hun mantel. De lange staart van zeepmoleculen wurmt zich in de mantel, waardoor deze uiteenvalt. Zonder beschermende mantel is het snel afgelopen met het inwendige RNA.
Verder kunnen we de ‘spike-eiwitten’ van het virion saboteren. Als hier antilichamen aan binden, kunnen ze geen cellen meer infecteren. Deze antilichamen worden gevormd bij immuniteit. Bijvoorbeeld na vaccinatie. Met kunstmatige, bijvoorbeeld monoklonale, antilichamen kunnen we het lichaam van de patiënt een handje helpen, als er nog geen immuniteit is en zo de coronavirions slopen.
Ook kunnen de ACE2-receptoren tijdelijk worden geblokkeerd, zodat het virus niet meer kan binden. Dit is gevaarlijk: de ACE2-receptoren regelen namelijk de bloeddruk. Schakelen we ze uit, dan stijgt die enorm.
Verhitting of straling beschadigt de manteleiwitten en het RNA in de kern. Dat schakelt het virion ook uit.
Binnen de cel ingrijpen is veel lastiger. We zouden het ribosoom anders, selectiever, kunnen inrichten, zodat het alleen menselijk messenger RNA vertaalt en virus-RNA negeert. Bijvoorbeeld door een bepaalde genetische code te vereisen. Dit vereist ingrijpende genetische manipulatie, met onbekende gevolgen. Ook zullen dan na verloop van tijd virussen evolueren, of, door kwaadwillenden worden samengesteld, die deze veiligheidsmaatregel kunnen omzeilen. Want, vergis je niet. Virussen samenstellen is al ruim 20 jaar mogelijk en wordt al routinematig gedaan voor onderzoeksdoeleinden.
Waarschijnlijk is goed handen wassen dan toch slimmer.





