Kan C4-fotosynthese de wereldvoedselproductie verdubbelen?
De plantenwereld kent twee belangrijke fotosynthesetechnieken: C3, de standaardmethode, en C4, waarbij de CO2 wordt geconcentreerd in de plant. C4 vaagt meer energie, maar de plant raakt veel minder snel in ‘ademnood’, waardoor de gewasopbrengsten in zonnige gebieden bijna twee keer zo hoog liggen. Kunnen we hiermee het wereldvoedselprobleem oplossen?

Hoe werkt fotosynthese?
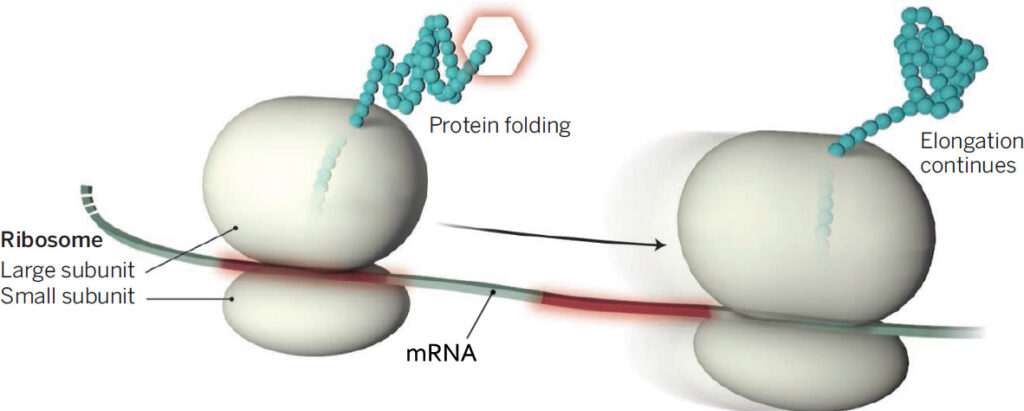
We hebben allemaal op school geleerd dat bladgroenkorrels licht opvangen, waar de plant voedsel mee maakt. Deze bladgroenkorrels vormen in feite alleen maar het begin van de keten. In de korrels wordt in de “lichtreactie” water gesplitst (waarbij als afvalproduct zuurstof vrijkomt) en waterstofionen (H+). Deze waterstofionen worden direct gebruikt om zes kooldioxidemoleculen (CO2) om te zetten in glucose (C6H12O6), de basisbouwstof voor plantencellen. Terwijl ze uit de bladgroenkorrel naar buiten worden gepompt, leveren deze ionen ook energie om ADP in de energiedrager ATP om te zetten.

Wat is het verschil tussen C3- en C4-fotosynthese?
Om het verschil tussen C3- en C4-fotosynthese uit te leggen, moeten we kijken naar de methode die de plant gebruikt om CO2 vast te leggen. Je zou het op grond van alle alarmverhalen niet zeggen, maar in feite verhongeren planten door te weinig CO2. Daarom bestaat de helft van alle eiwitten bij planten uit maar één enzym: rubisco, het enzym dat CO2 vangt en inbouwt in de zogeheten Calvin-cyclus. Dit enzym is miljarden jaren geleden ontstaan, toen er nog geen zuurstof in de atmosfeer zat. Daarom is het niet berekend op de aanwezigheid van zuurstof, waardoor er veel CO2 verloren gaat. In plaats van rubisco te veranderen, wat voor een plant zelfmoord zou betekenen, ontstonden naast de standaard (C3) vorm van fotosynthese, twee extra methoden om te voorkomen dat er teveel zuurstof bij het rubisco in de buurt komt: C4-metabolisme en CAM.
CAM-planten, zoals cactussen, zetten hun huidmondjes ’s nachts open en vangen dan CO2 (die ze opslaan in appelzuur), die ze overdag weer afsplitsen en verder verwerken. Deze strategie kost veel energie, maar spaart water en komt daarom vooral voor bij woestijnplanten, waarvoor water veel belangrijker is dan energiebesparing.
We hebben het hier verder over C4-planten. Deze planten gebruiken een andere techniek: het huisvesten van Rubisco in een CO2-rijke omgeving. Dit krijgen deze planten voor elkaar, door CO2 in twee stappen vast te leggen. In de eerste stap, in een krans om de cellen waar de donkerreactie plaatsvindt, wordt CO2 vastgelegd in een verbinding met 4 koolstofatomen (vandaar de naam C4), die wordt getransporteerd naar de plek waar Rubisco het verwerkt. Daardoor gaat er minder energie verloren. Wel kost dit proces 30 ATP, waar de ‘normale’ C3-fotosynthese maar 18 ATP kost. Bekende C4-gewassen zijn maïs, suikerriet en sorghum (hier minder bekend, maar in Afrika een van de belangrijkste voedingsgewassen). C4-planten evolueerden rond de 30 miljoen jaren geleden, toen de CO2-hongersnood nijpend werd en het klimaat droger werd.
Tarwe, rijst en andere gewassen ombouwen tot C4-plant
Maïs en sorghum zijn minder populair als voedselgewas dan tarwe en rijst. Hoewel in de tropen de opbrengsten van maïs veel groter zijn dan die van rijst, kiezen boeren daarom toch massaal voor rijstteelt. Zouden we er in slagen om C4-eigenschappen in deze populaire voedingsgewasssen in te bouwen, dan zouden we de oogsten per hectare met 50% kunnen vergroten. Terwijl er minder kunstmest en water nodig is, waardoor per liter water de oogst verdrievoudigt. Voor woestijnlanden als Egypte en dichtbevolkte landen als India, Nigeria en Bangladesh zou dit uiteraard een uitkomst zijn. Toch vrees ik dat de smaak iets achteruit zal gaan. Voor C4 moeten er kransen om de plekken waar de Calvin-reactie plaatsvindt worden aangemaakt. De reden dat typische C4-granen als sorghum en maïs een vrij harde smaak hebben, is vermoedelijk die laag.Aan de andere kant: we hebben weinig keus meer. De watertekorten over de gehele wereld worden steeds nijpender en in gebieden als Californië stijgt de rijstoogst al niet meer sinds 1990. Op dit moment is het implanteren van het C4-mechanisme in voedselgewassen onze beste hoop om wereldwijd voedselgebrek te voorkomen.
Het C4-rijstproject
Het internationale rijst-onderzoeksinstituut IRRI in de Filippijnen is daarom begonnen met het ontwikkelen van een C4-variant van rijst. Dit project, met 5 miljoen dollar gefinancierd door de eBill and Melinda Gates Foundation, moet in een jaar of zes tot tien een bruikbare cultivar opleveren. Deze variant zal veel minder water gebruiken en een wat grotere oogst per hectare opleveren. Gezien het enorme belang van de voedselvoorziening is het onbegrijpelijk dat er zo weinig hulpbronnen in dit project worden gestopt. De taak die de onderzoekers te wachten staat is wanhopig moeilijk. Ze moeten de bestaande genen van rijst zo wijzigen, dat zich concentrische ringen van cellen gaan vormen. Als je bedenkt, dat in genen alleen eiwitten staan beschreven, niet direct de anatomie van planten, kan je je voorstellen dat dit een enorm veeleisende taak is. Toch slaagden planten hier in meer dan dertig plantensoorten in, weten we. Toch is het ze nu gelukt het rudimentaire C4-proces in rijst in te bouwen. Uiteraard moet deze rijst nog doorontwikkeld worden in een levensvatbaar C4-ras, maar er is nu voor het eerst zicht op een structurele oplossing.
Bronnen
Supercharged photosynthesis, MIT Review,2015









![Een eiwit met polymeerjas blijkt te kunnen werken zonder water. Is dan toch leven zonder water mogelijk? Bron: [1]](https://www.visionair.nl/wp-content/uploads/2012/08/eiwit-met-jas.jpg)